专业赋能医疗器械企业,构建合规高效的质量管理体系
一、ISO 13485标准简介
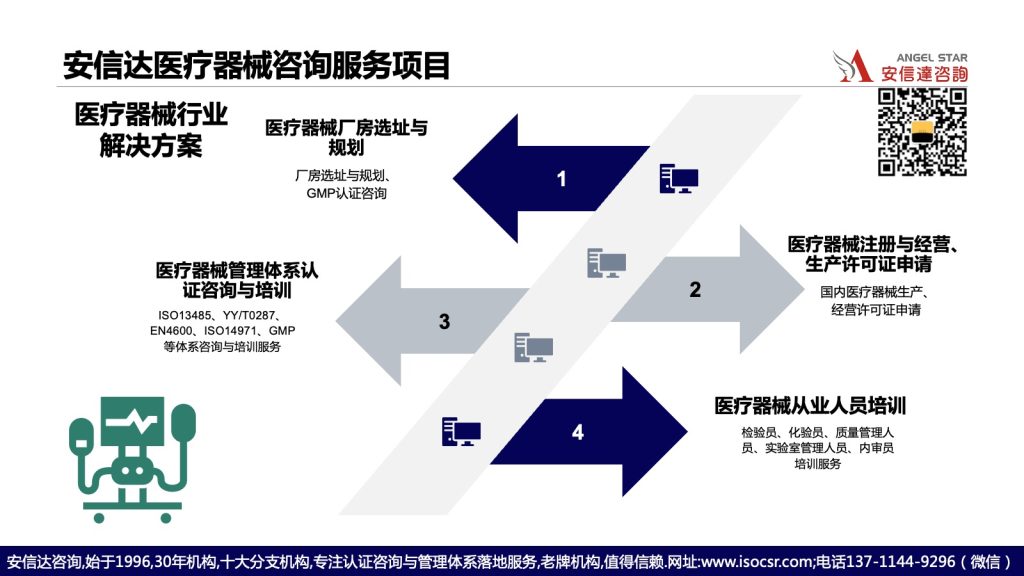
ISO 13485是国际标准化组织(ISO)发布的医疗器械行业质量管理体系标准,全称为《医疗器械 质量管理体系 用于法规的要求》。其核心目标是帮助企业在医疗器械设计、开发、生产、安装及服务全生命周期中,建立符合法规要求的质量管理体系,确保产品安全有效。
标准特点:
1. 法规导向:强调医疗器械注册、生产许可等法规要求,是进入欧盟(CE)、美国(FDA)等国际市场的准入门槛。
2. 风险管理:要求贯穿产品全生命周期的风险分析(如FMEA、风险管理计划),降低质量事故概率。
3. 文件化要求:明确需建立20余类文件(如质量手册、程序文件、验证报告),确保过程可追溯。
4. 适用性广泛:覆盖医疗器械设计、生产、灭菌、流通及服务,适用于二类、三类器械企业及供应商。
二、ISO 13485认证要求
企业申请认证需满足以下核心条件:
1. 资质要求:
• 合法营业执照及医疗器械生产/经营许可证(二类、三类必备)。
• 产品注册证或备案凭证(如植入物需提供国家药监局审批文件)。
2. 体系运行时间:
• 三类器械:体系运行≥6个月;其他器械≥3个月。
• 需完成至少一次内部审核和管理评审。
3. 文件完备性:
• 质量手册、程序文件、风险管理报告、灭菌验证记录等20余类材料。
4. 合规记录:
• 申请前1年内无重大质量事故或客户投诉。
三、ISO 13485认证流程
安信达咨询提供全流程闭环服务,确保高效通过认证:
1. 初次认证
• 阶段1:诊断评估
• 现场调研企业现有体系,识别与ISO 13485的差距(如文件缺失、流程漏洞)。
• 阶段2:体系构建
• 定制化编制质量手册、程序文件及记录表单,融入风险管理工具(FMEA/FTA)。
• 阶段3:内审与改进
• 培训内审员,开展内部审核,针对不符合项制定纠正措施。
• 阶段4:认证审核
• 配合第三方认证机构(如SGS、TÜV)完成文件评审与现场审核,获取证书。
2. 年度监督审核
• 每年一次现场检查,重点审查体系持续有效性及改进措施落实情况。
3. 复评认证
• 证书到期前3个月启动,重新评估体系与最新法规的符合性。
四、安信达咨询的核心优势
1. 行业深耕,经验丰富
• 成立于1996年,国内首批提供ISO13485咨询和培训的专业机构,累计服务超1000家医疗器械企业。
• 覆盖高风险器械(III类植入物)、体外诊断设备等细分领域,提供定制化解决方案。
2. 专业团队,全程护航
• 200+签约咨询师,均具备15年以上医疗器械行业经验,持有各类咨询、审核与培训资质证书。
• 提供“标准培训→体系搭建→内审辅导→认证申请”全链条服务,确保零基础企业快速达标。
3. 本地化服务,高效响应
• 全国多地分支机构,支持现场办公、远程协作,紧急问题24小时内响应。
• 提供“认证+法规更新”联动服务,实时跟踪NMPA、FDA等政策变化。
4. 成功案例,实力见证
• 助力迈瑞医疗、华大基因、理邦医疗、尚荣医疗、稳健医疗、鱼跃医疗、飞利浦、3M等国内外企业通过认证及提供人员提升培训服务。
• 提供免费试讲、案例复盘,确保企业内审员掌握风险管理、CAPA等核心技能。
5. 熟悉机构
• 与审查中心、国内外各大认证机构(如SGS,TUV,BS,BSI,DNV,NQA,华光,CQC)等保持良好的合作关系,更熟悉认证规则与审核要求
五、选择安信达的三大理由
资历经验:始于1996,30年老牌机构,资深服务团队,千余家企业服务经验。
合规保障:确保企业符合国内及国际法规及标准。
成本优化:通过流程精简与风险预防,降低质量事故损失。
市场赋能:认证证书成为招投标、海外合作的“硬通货”,提升品牌公信力。
安信达咨询以专业、高效、合规为核心,助力企业构建国际一流的质量管理体系,抢占全球医疗器械市场先机!
ISO13485认证咨询热线,137-1144-9296(微信) 孙经理

安信达咨询

医疗器械认证咨询

安信达咨询合作认证机构

安信达咨询